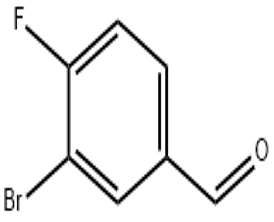
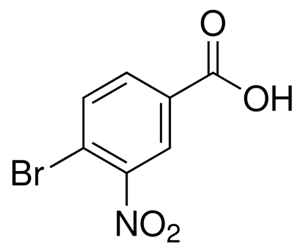
alfa-ionon(CAS#127-41-3)
| Risikokoder | R42/43 – Kan give overfølsomhed ved indånding og hudkontakt. |
| Sikkerhedsbeskrivelse | S24/25 – Undgå kontakt med hud og øjne. |
| WGK Tyskland | 2 |
| RTECS | EN0525000 |
| TSCA | Ja |
| HS kode | 29142300 |
alfa-ionon(CAS#127-41-3) oplysninger
Violet keton, også kendt som benzophenon, er en organisk forbindelse. Her er nogle sikkerhedsoplysninger om ionon:
1. Toksicitet: Violet keton har en vis toksicitet for den menneskelige krop. Det kan forårsage skade på centralnervesystemet og leveren og kan have negative virkninger på det reproduktive system og embryoner.
2. Indåndingsfare: Indånding af dampe eller støv fra ionon kan forårsage ubehagssymptomer såsom svimmelhed, døsighed, hoste og åndedrætsbesvær. Langtidseksponering kan forårsage skade på centralnervesystemet.
3. Kontaktfare: Violet keton kan absorberes gennem huden. Langvarig eller omfattende kontakt kan forårsage hud- og øjenirritation. Passende personlige værnemidler såsom handsker og sikkerhedsbriller bør bæres ved håndtering af ionon.
4. Brandslukningsforanstaltninger: I tilfælde af lækage eller brand, brug tørt pulver, skum eller kuldioxid til at slukke branden. Undgå at bruge vand, da violet keton reagerer med vand og danner brændbare gasser.
5. Bortskaffelse af affald: Bortskaf affaldet violet keton korrekt i overensstemmelse med lokale regler og regler. Udled det ikke i kloakken eller skraldespanden.
6. Forholdsregler ved opbevaring: Violet keton skal opbevares på et køligt, tørt, godt ventileret sted, væk fra brandkilder og oxidanter.
Disse oplysninger er kun til reference. Hvis yderligere brug eller forarbejdning af ionon er påkrævet, henvises til det relevante sikkerhedsdatablad og konsulter en professionel.
natur
Violet keton, også kendt som linaylketon, er en naturlig ketonforbindelse. Det er hovedbestanddelen af aromaen af violette blomster.
Violet keton er en farveløs til bleggul olieagtig væske, der er flygtig ved stuetemperatur.
Violet keton er opløseligt i alkohol og etheropløsningsmidler og let opløseligt i vand. Dens massefylde er relativt lav med en massefylde på 0,87 g/cm³. Det er følsomt over for lys og kan absorbere ultraviolette stråler.
Violet keton kan oxideres til ketonalkoholer eller syrer i kemiske reaktioner og kan reduceres til alkoholer gennem hydrogeneringsreduktionsreaktioner. Det kan gennemgå alkylerings- og esterificeringsreaktioner med mange forbindelser.
Anvendelse og syntesemetode
Violet keton (også kendt som lilla keton) er en aromatisk ketonforbindelse. Den har en speciel duft og bruges ofte i parfume- og parfumeindustrien. Det følgende er en introduktion til anvendelser og syntesemetoder af ionon:
Formål:
Parfume og krydderier: duftegenskaberne af ionon, som er meget brugt i parfume- og krydderiindustrien til fremstilling af violet duftprodukter.
Syntesemetode:
Syntesen af ionon opnås generelt gennem følgende to metoder:
Oxidation af nukleobenzen: Nukleobenzen (en benzenring med en methylsubstituent) udsættes for en oxidationsreaktion, såsom at bruge en oxiderende syre eller en sur kaliumpermanganatopløsning, for at generere ionon.
Kobling af pyrylbenzaldehyd: Pyrylbenzaldehyd (såsom benzaldehyd med pyridinringsubstituenter i para- eller metapositionen) omsættes med eddikesyreanhydrid og andre reaktanter under alkaliske betingelser for at danne ionon.